1. Global byrde av livmorhalskreft og screeningutfordringer
Livmorhalskreft er fortsatt en stor global folkehelseutfordring, til tross for at den i stor grad kan forebygges gjennom effektiv screening og tidlig intervensjon. Ifølge Verdens helseorganisasjon (WHO) var det anslått 662 000 nye tilfeller og 349 000 dødsfall over hele verden i 2022, noe som rangerer den som den fjerde vanligste kreftformen og den fjerde ledende årsaken til kreftrelatert dødelighet blant kvinner. Sykdomsbyrden er uforholdsmessig konsentrert i lav- og mellominntektsland (LMIC-er), hvor forekomst og dødelighet er betydelig høyere enn i høyinntektsland. Dette skyldes først og fremst mangel på screeningprogrammer av høy kvalitet og effektiv deteksjon og behandling av precancerøse lesjoner, forverret av:
-Mangel på eller svak screeninginfrastruktur:Mangel på tilgjengelige, kvalitetssikrede screeningstjenester.
-Ressursbegrensninger:Begrenset laboratorieinfrastruktur, kjølekjedelogistikk og pålitelig strøm.
-Mangel på arbeidskraft:Mangel på trent laboratorie- og klinisk personell.
-Forsinkelser og tap av oppfølging:Forsinkelse mellom prøveinnsamling og tilgjengeligheten av resultater, noe som fører til forsinkelser i klinisk behandling eller at pasienter går tapt for oppfølging[1].
2. Etiologi og molekylært grunnlag for livmorhalskreft
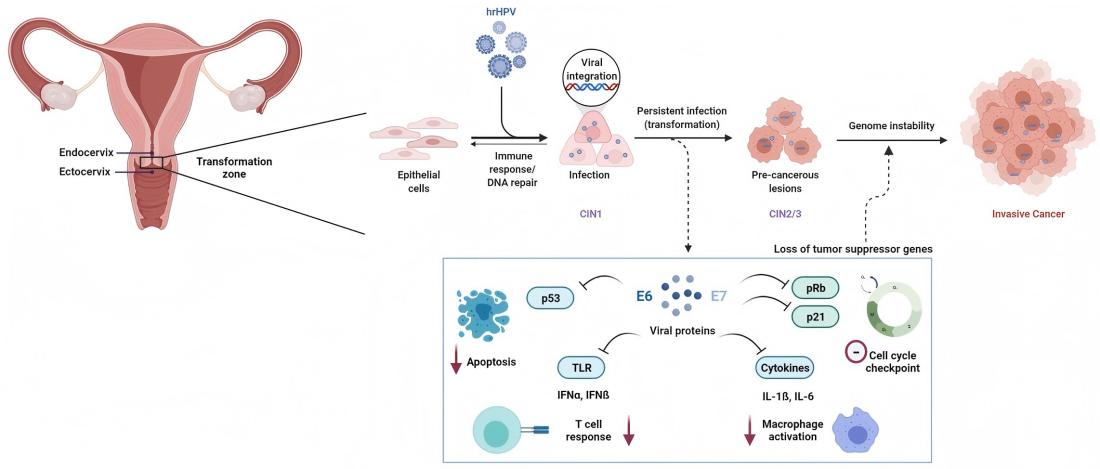
Vedvarende infeksjon med høyrisiko humant papillomavirus (HR-HPV) er en nødvendig årsak til livmorhalskreft. Blant mer enn 200 identifiserte HPV-genotyper har minst 12 typer blitt klassifisert som kreftfremkallende (gruppe 1) av Det internasjonale byrået for kreftforskning (IARC).
På molekylært nivå er HPV-mediert karsinogenese primært drevet av de virale onkoproteinene E6 og E7. E6 fremmer nedbrytningen av tumorsuppressorproteinet p53, mens E7 funksjonelt inaktiverer retinoblastomproteinet (Rb), noe som resulterer i dysregulering av cellesyklusen og malign transformasjon.
3. WHO-anbefalte screeningstrategier
Verdens helseorganisasjon anbefaler HPV-nukleinsyretesting (NAT) som den foretrukne primærscreeningmetoden for forebygging av livmorhalskreft.
Generell befolkning:HPV DNA- eller mRNA-baserte NAT-er
Kvinner som lever med hiv:HPV DNA-baserte NAT-er
Screeningintervaller:
Kvinner i alderen 30–65 år: Hvert 5.–10. år
Kvinner som lever med hiv: Hvert 3.–5. år
Sammenlignet med cytologibaserte metoder viser HPV-testinghøyere følsomhetog giren overlegen negativ prediktiv verdi, noe som muliggjør lengre og mer kostnadseffektive screeningsintervaller.
4. WHOs målproduktprofil for HPV-screeningtester
WHO har utviklet enMålproduktprofil (TPP)for HPV-screeninganalyser beregnet for bruk i desentraliserte og ressursbegrensede miljøer.[1]
Viktige egenskaper inkluderer:
-Kompatibilitet med selvinnsamlede prøver
-Påvisning av flere høyrisiko HPV-genotyper (≥12 typer)
-Bruk av personell uten laboratorieopplæring
-Resultater tilgjengelige innen ett enkelt klinisk møte
Disse kriteriene støtter pasientnær testing og «screen-and-treat»-strategier.
5. En helautomatisert plattform for deteksjon av HPV med høy risiko
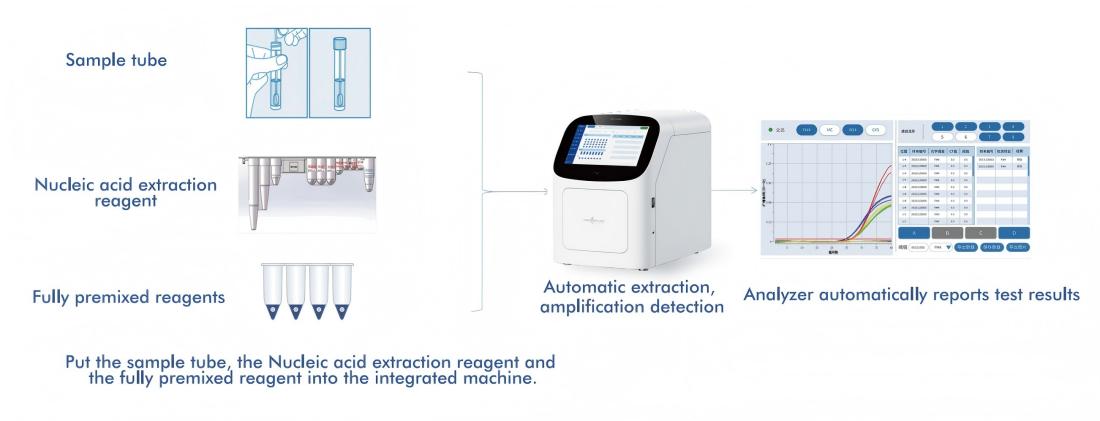
Macro & Micro-Tests AIO800-system giren helautomatisert arbeidsflyt fra eksempel til svarintegrering av nukleinsyreekstraksjon, amplifisering og deteksjon i tråd med WHO-anbefalte screeningstrategier.
5.1 Automatisert arbeidsflyt fra prøve til svar
Plattformen integrerer nukleinsyreekstraksjon, amplifisering og deteksjon i et enkelt, lukket system, som krever minimal operatørinngripen. Denne designen:
-Reduserer avhengigheten av spesialisert laboratoriepersonell
-Minimerer prosessvariabilitet og forurensningsrisiko
-Muliggjør utplassering i desentraliserte helsemiljøer
Samtidig støtter gjennomstrømningskapasiteten bruk i sentraliserte laboratorier, noe som legger til rette for storskala screeningprogrammer.
5.2 Bred genotypingsdekning
Systemet oppdager 14 HPV-typer med høy risiko, inkludert alle 12 kreftfremkallende typer klassifisert av IARC (HPV16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58 og 59), samt HPV66 og HPV68.
Viktigst av alt, det girtypespesifikk genotypingresultater, noe som muliggjør risikostratifisering og mer presis klinisk behandling.
5.3 Analytisk sensitivitet og kliniske implikasjoner
Med en deteksjonsgrense på 300 kopier/ml er systemet i stand til å identifisere lavnivå-HPV-infeksjon som bidrar til:
-Tidligere deteksjon av klinisk relevante infeksjoner
-Forbedret negativ prediktiv verdi
-Støtte for utvidede screeningsintervaller
5.4 Støtte for selvprøvetaking
Plattformen er kompatibel med beggelivmorhalsprøver og selvinnsamlede urinprøveri samsvar med WHOs anbefalinger for å håndtere viktige barrierer for screeningopptak, inkludert:
-Begrenset tilgang til helsefasiliteter
-Sosiokulturelle begrensninger
-Pasientens ubehag ved klinikerbasert prøvetaking
Selvprøvetaking har vist seg å øke deltakelsen i screeningprogrammer, spesielt blant underforsynte befolkningsgrupper.
5.5 Lyofilisert reagensteknologi for lagring i romtemperatur
For ytterligere å forbedre anvendeligheten i ressursbegrensede situasjoner, inkluderer systemetfrysetørkede reagensersom er stabile ved romtemperatur, og gir flere driftsfordeler:
- Uavhengighet av kjølekjeden: Eliminerer behovet for kjøletransport og -lagring
-Forbedret stabilitet: Opprettholder reagensintegriteten under varierende miljøforhold
-Forenklet logistikk: Reduserer infrastrukturbehov og driftskostnader
-Forbedret tilgjengelighet: Forenkler utplassering i avsidesliggende eller underforsynte regioner
6. Konklusjon
Overgangen fra cytologibasert screening til HPV-basert molekylær testing representerer et paradigmeskifte innen forebygging av livmorhalskreft. Ved å målrette den underliggende årsaken til sykdommen snarere enn morfologiske endringer, muliggjør HPV-testingtidligere og mer sensitiv deteksjonav risikoutsatte individer.
Dessuten tilbyr de helautomatiske molekylærdiagnostiske plattformene en praktisk tilnærming for å overvinne eksisterende barrierer i screeninglevering. Ved å kombinerehøy analytisk ytelse med enkel drift og støtte for selvprøvetaking,AIO800 har potensial til å utvide screeningsdekningen, forbedre tidlig deteksjon og bidra til å redusere den globale byrden av livmorhalskreft.
Referanser:
1. Verdens helseorganisasjon. Målrettede produktprofiler for screeningtester for humant papillomavirus for å oppdage prekreft og livmorhalskreft. Genève: WHO; 2024.
Publisert: 28. mars 2026