Nylig publiserte British Journal of Clinical Pharmacology den første kliniske retningslinjen utviklet av UK Centre of Excellence for Regulatory Science and Innovation in Pharmacogenomics (CERSI PGx), med tittelen «CYP2C19 genotype testing for clopidogrel: A guideline developed by the UK Centre of Excellence for regulatory science and innovation in pharmacogenomics (CERSI PGx)». Dette milepælsdokumentet fokuserer på den kliniske verdien av CYP2C19 genotyping i veiledning av klopidogrelbehandling.

Om CERSI PGx
CERSI PGx er et av syv britiske myndighetsstøttede sentre for regulatorisk vitenskap og innovasjon som ble lansert i januar 2025. Det ledes av University of Liverpool og er i fellesskap finansiert av Innovate UK, Medical Research Council (MRC), Medicines and Healthcare products Regulatory Agency (MHRA) og Office for Life Sciences (OLS). Senteret har som mål å akselerere den sikre og effektive integreringen av farmakogenomikk (PGx) i National Health Service (NHS) ved å adressere viktige implementeringsbarrierer. Denne retningslinjen markerer den aller første kliniske veiledningen som er utstedt siden CERSI PGx ble etablert.
Hvorfor CYP2C19 er viktig for klopidogrel
CYP2C19 er et sentralt medlem av cytokrom P450-enzymfamilien, ansvarlig for metabolsk aktivering eller inaktivering av mange legemidler. Genetiske polymorfismer i CYP2C19 fører til betydelige interindividuelle forskjeller i legemiddelmetabolisme, noe som påvirker effekt og sikkerhet.
Klopidogrel er et mye brukt platehemmende middel for å forebygge trombotiske hendelser ved koronar arteriesykdom, iskemisk hjerneslag, perifer arteriesykdom og atrieflimmer. Som et prodrug krever klopidogrel metabolsk aktivering av CYP2C19. Retningslinjene klassifiserer individer i ultraraske, raske, normale, intermediære og dårlige metaboliserere basert på CYP2C19-genotypen. Bærere av funksjonstapsalleler (f.eks. CYP2C192 og *3*) – intermediære og dårlige metaboliserere – kan ikke effektivt aktivere klopidogrel, noe som fører til utilstrekkelig platehemming og økt risiko for tilbakevendende trombose.
Frekvensen av CYP2C192-allelet er omtrent 15 % hos europeere, 30 % hos sør-asiater og så høy som 60 % i urbefolkninger i Oseania.
Viktigste anbefaling: Universell CYP2C19-testing for klopidogrel
Retningslinjen sier at uansett indikasjon, bør alle pasienter som vurderer klopidogrelbehandling for gjennomgåCYP2C19genotyping.Basert på resultatene bør platehemmende behandling optimaliseres:
-Dårlige metabolisererebør unngå klopidogrel og fortrinnsvis bruke alternative legemidler som ikke er avhengige av CYP2C19-metabolisme, som ticagrelor eller prasugrel.
-Intermediære metabolisererebør også vurdere alternative midler eller justerte behandlingsregimer i stedet for bare å øke klopidogreldosen.
I Storbritannia er klopidogrel godkjent for sekundærforebygging av aterotrombotiske hendelser, for moderat til høy risiko for transitorisk iskemisk anfall (TIA) eller mildt iskemisk hjerneslag, og for å forebygge aterotrombotiske og tromboemboliske hendelser ved atrieflimmer.
Utover klopidogrel: Andre legemidler der CYP2C19-genotyping er kritisk
Verdien av CYP2C19-genotyping strekker seg langt utover klopidogrel. Som et viktig legemiddelmetaboliserende enzym spiller CYP2C19 også en kritisk rolle i metabolismen av vorikonazol, flere antidepressiva og protonpumpehemmere (PPI-er). Flere internasjonale og nasjonale retningslinjer anbefaler genotypestyrt individualisering for disse legemidlene.
1. Antidepressiva (SSRI-er)
Selektive serotoninreopptakshemmere (SSRI-er) – som sertralin, citalopram og escitalopram – er førstelinjemidler mot depresjon og metaboliseres primært av CYP2C19. CYP2C19-enzymaktiviteten bestemmer direkte plasmakonsentrasjonen av disse legemidlene. Langsomme metaboliserere har en reduksjon i legemiddelclearance på 30–60 %, noe som predisponerer dem for bivirkninger som forlengelse av QT-intervallet og sedasjon. Ultraraske metaboliserere har ofte subterapeutiske plasmakonsentrasjoner, noe som fører til forsinket behandlingsrespons og økt risiko for seponering av legemidlet.
Retningslinjene fra Clinical Pharmacogenetics Implementation Consortium (CPIC) fra 2023 slår fast at personer med lav metabolisering som tar citalopram eller escitalopram har økt risiko for QT-forlengelse, og anbefaler en dosereduksjon på 50 %. Retningslinjene fra Dutch Pharmacogenetics Working Group (DPWG) fra 2021 anbefaler at personer med lav metabolisering bør få en maksimal dose escitalopram redusert med 50 %, og at personer med ultraraske metabolisering bør unngå escitalopram helt. For sertralin anbefaler DPWG en daglig dose som ikke overstiger 75 mg hos personer med lav metabolisering.
Det er viktig å merke seg at den nylig publiserte kinesiske ekspertkonsensusen om farmakogenomisk testing i psykiatri (2025) – utviklet av Precision Medicine Collaboration Group i det kinesiske psykiatriske selskapet – eksplisitt inkluderer anbefalinger for genotyping av CYP2C19. Konsensusuttalelsen bemerker at anbefalinger for dosejustering fra internasjonale retningslinjer som CPIC og DPWG for legemiddelmetaboliserende enzymer (inkludert CYP2C19) kan refereres til for kinesiske befolkninger. Derfor muliggjør CYP2C19-genotyping før oppstart av SSRI-behandling (f.eks. escitalopram) doseoptimalisering eller bytte til alternative legemidler som ikke metaboliseres av CYP2C19, og dermed oppnår presisjonsbehandling, forbedrer responsrater og reduserer bivirkninger.
2. Protonpumpehemmere (PPI-er)
Protonpumpehemmere – inkludert omeprazol, lansoprazol og pantoprazol – er mye brukt for syrerelaterte lidelser som gastroøsofageal reflukssykdom og magesår. Metabolismen deres er også svært avhengig av CYP2C19. Pasienter med forskjellige CYP2C19-genotyper viser betydelig variasjon i respons på PPI-er. Bærere av funksjonstapsalleler (*2, *3) har markant økt legemiddeleksponering, noe som kan forsterke syresuppresjonen, men også øke risikoen for bivirkninger. I motsetning til dette har normale metaboliserere relativt lavere plasmakonsentrasjoner og kan oppleve svakere syresuppresjon, selv om variasjonen mellom individuelle legemidler fortsatt er betydelig.
CPIC-retningslinjene for PPI-er fra 2020 anbefaler at ultrahurtige metaboliserere som tar omeprazol eller lignende legemidler metaboliserer legemidlet for raskt, noe som resulterer i utilstrekkelige plasmakonsentrasjoner og dårlig syresuppresjon. Hos disse pasientene bør dosen økes og den terapeutiske responsen overvåkes. For langsomme metaboliserere er legemiddelclearance langsom og plasmakonsentrasjonene kan være forhøyede. Selv om effekten kan være bedre, øker potensialet for legemiddeltoksisitet. Dosereduksjon og overvåking av respons er rimelige hensyn. Derfor anbefales CYP2C19-genotyping for pasienter som starter PPI-behandling eller de som opplever dårlig respons eller bivirkninger for å veilede individualisert dosering, optimalisere effekt og minimere bivirkninger.
3. Vorikonazol
Vorikonazol er et bredspektret soppdrepende middel som brukes til å behandle alvorlige soppinfeksjoner som invasiv aspergillose. Det har et smalt terapeutisk vindu: for høye plasmakonsentrasjoner øker risikoen for levertoksisitet og synsforstyrrelser, mens lave konsentrasjoner fører til behandlingssvikt. Metabolismen av vorikonazol medieres primært av CYP2C19, og genetiske polymorfismer har en betydelig innvirkning på plasmakonsentrasjonen.
CPIC publiserte en egen retningslinje om CYP2C19 og vorikonazol i 2016. Den slår fast at ultraraske metaboliserere har reduserte bunnkonsentrasjoner av vorikonazol og ofte ikke når målterapeutiske nivåer. Dårlige metaboliserere har forhøyede bunnkonsentrasjoner og en betydelig økt risiko for bivirkninger. CPIC-retningslinjene gir spesifikke doseringsanbefalinger basert på genotype. For eksempel bør voksne ultraraske metaboliserere få alternative førstelinjemidler som ikke er avhengige av CYP2C19-metabolisme, som isavukonazol, liposomalt amfotericin B eller posakonazol. Derfor muliggjør CYP2C19-genotyping før vorikonazolbehandling individualisert dosering og reduserer forekomsten av legemiddelrelaterte bivirkninger.
Klinisk betydning: Gjør medisiner mer pålitelige
Den nylig utgitte retningslinjen plasserer nok en gang CYP2C19-genotyping i forkant av presisjonsmedisin. Det er imidlertid viktig å erkjenne at de kliniske anvendelsene av CYP2C19-genotyping går langt utover klopidogrel – fra vorikonazol (soppdrepende middel) og SSRI-er (antidepressiva) til protonpumpehemmere for syresuppresjon. CYP2C19-genotypen fungerer som et «kompass» for medikamentell behandling.
Etter hvert som presisjonsmedisin får bredere aksept, innlemmer et økende antall autoritative retningslinjer CYP2C19-genotyping i rutinemessige medisineringsarbeidsflyter. For pasienter hjelper det å kjenne sin egen CYP2C19-genotype dem med å forstå sin individuelle legemiddelresponsprofil og muliggjør delt beslutningstaking med legen sin for å utvikle en mer passende behandlingsplan. For klinikere er integrering av objektive genetiske testresultater i forskrivningsbeslutninger et kraftig middel for å forbedre behandlingskvaliteten og sikre pasientsikkerhet.
Makro- og mikrotest'sCYP2C19 genotypingsløsning
Macro & Micro Test tilbyr et CYP2C19 genotypingssett basert på et forbedret amplifiseringsrefraktært mutasjonssystem (ARMS) kombinert med Taqman-prober med følgende funksjoner:
-Omfattende alleldekning– oppdagerCYP2C192, *3 og *17uten å mangle viktige varianter.
-Robust kvalitetskontroll– inneholder negative/positive kontroller, en intern kontroll og UDG-enzym for firenivås kvalitetskontroll for å sikre nøyaktige resultater.
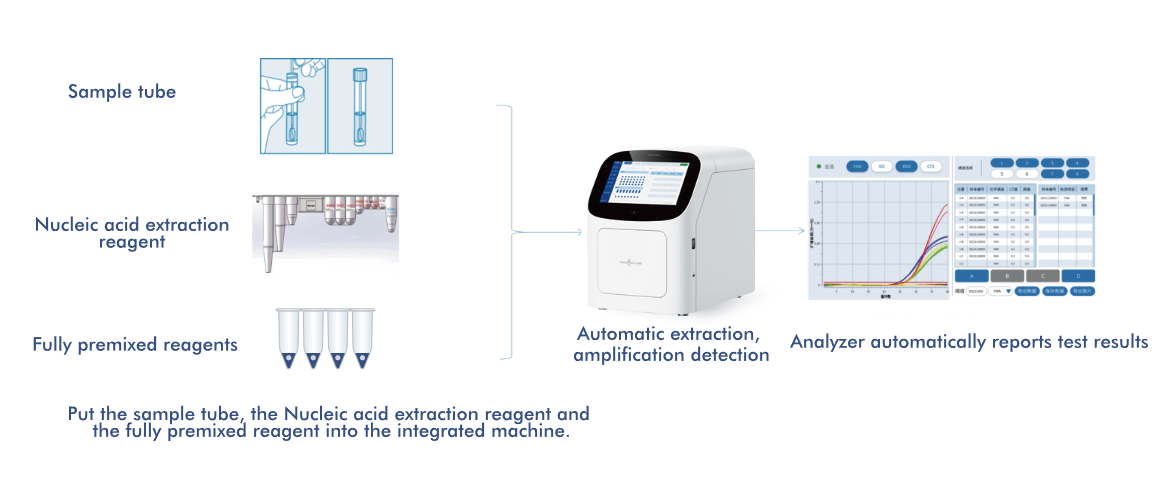
-Automatisert utvinning– kompatibel med Macro & Micro-Tests helautomatiske nukleinsyreekstraktor, noe som forbedrer arbeidsflyteffektiviteten.
-Bred kompatibilitet– fungerer med vanlige sanntids-PCR-instrumenter på markedet, inkludert ABI 7500 Hongshi SLAN 96P.
-Automatisert tolkning av resultater– dedikert analyseprogramvare (på ABI 7500, SLAN 96P, osv.) muliggjør automatisk tolkning av resultater, noe som forbedrer effektiviteten.
-POCT-klar automatisering– HWTS AIO800 helautomatisk nukleinsyreamplifiseringsanalysator muliggjør «prøve inn, resultat ut»-drift.
Med den kontinuerlige utviklingen innen farmakogenomikk forventes det at CYP2C19-genotyping vil være til fordel for et økende antall pasienter, og flytte presisjonsmedisin fra konsept til rutinemessig klinisk praksis. Den nylig publiserte CERSI PGx-retningslinjen forsterker den kritiske rollen til CYP2C19-testing, ikke bare for klopidogrel, men også for en voksende liste med legemidler, inkludert antidepressiva, protonpumpehemmere og vorikonazol. For å legge til rette for utbredt bruk av genotypestyrt forskrivning er pålitelige og brukervennlige testløsninger avgjørende. Macro & Micro-Tests portefølje for farmakogenomisk testing, med omfattende alleldekning, robust kvalitetskontroll og automatiseringsklare plattformer, har som mål å støtte helsepersonell i å implementere presisjonsmedisin og til syvende og sist ivareta pasientenes helse.
Relaterte produkter:
Referanser:
1. Lima JJ, Thomas CD, Barbarino J, et al. Retningslinje fra Clinical Pharmacogenetics Implementation Consortium (CPIC) for dosering av CYP2C19 og protonpumpehemmere. Clin Pharmacol Ther. 2020. doi:10.1002/cpt.20151.
2. Lee CR, Luzum JA, Sangkuhl K, et al. Retningslinje for implementering av klinisk farmakogenetikk for CYP2C19-genotype og klopidogrelbehandling: 2022-oppdatering. Clin Pharmacol Ther. 2022. doi:10.1002/cpt.25261.
3. National Institute for Health and Care Excellence (NICE). CYP2C19-genotypetesting for å veilede bruk av klopidogrel etter iskemisk hjerneslag eller transitorisk iskemisk anfall. Diagnostisk veiledning DG59. Publisert: 31. juli 2024.
4. Samarbeidsgruppen for presisjonsmedisinsk forskning i det kinesiske psykiatriske selskapet. Ekspertkonsensus om farmakogenomisk testing i psykiatri (2025) [Zhonghua Jing Shen Ke Za Zhi].Kinesisk tidsskrift for psykiatri. 2025;58(6):434–445. doi:10.3760/cma.j.cn11366120240611-00181
5. Dello Russo C, Frater I, Kuruvilla R, et al. CYP2C19 genotypetesting for klopidogrel: En retningslinje utviklet av UK Centre of Excellence for regulatory science and innovation in pharmacogenomics (CERSI-PGx). Br J Clin Pharmacol. 2025. DOI: 10.1093/bjcp/…
6. Moriyama B, Owusu Obeng A, Barbarino J, et al. Retningslinjer fra Clinical Pharmacogenetics Implementation Consortium (CPIC) for CYP2C19- og vorikonazolbehandling. Clin Pharmacol Ther. 2017;102(1):45-51. doi:10.1002/cpt.595.
7. Bousman CA, Stevenson JM, Ramsey LB, et al. Retningslinje fra Clinical Pharmacogenetics Implementation Consortium (CPIC) for genotypene CYP2D6, CYP2C19, CYP2B6, SLC6A4 og HTR2A samt serotoninreopptakshemmere som antidepressiva. Clin Pharmacol Ther. 2023;114(1):51-68. doi:10.1002/cpt.2903.
8. Brouwer JMJL, Nijenhuis M, Soree B, et al. Retningslinje fra den nederlandske arbeidsgruppen for farmakogenetikk (DPWG) for gen-legemiddel-interaksjonen mellom CYP2C19 og CYP2D6 og SSRI-er. Eur J Hum Genet. 2021. doi:10.1038/s41431-021-00894-2.
Publisert: 22. april 2026