24. mars 2026 markerer den 31. Verdens tuberkulosedag. Verdens helseorganisasjon (WHO) har annonsert årets globale tema som«Ja! Vi kan få slutt på tuberkulose!», og understreker at sterkt myndighetsledelse, vedvarende politisk engasjement og koordinert tverrsektoriell handling er avgjørende for å få slutt på tuberkuloseepidemien (TB).

Global fremgang og gjenværende utfordringer
Ifølge den globale tuberkuloserapporten fra 2025 nådde global tuberkulosekontroll en betydelig milepæl i 2024, med både iforekomst og dødelighet synkendefor første gang siden COVID-19-pandemien.
Et anslag10,7 millioner menneskerutviklet tuberkulose i 2024, inkludert 54 % menn, 35 % kvinner og 11 % barn og ungdom. Blant disse tilfellene var omtrent619 000 (5,8 %)var samtidig smittet med HIV, og390 000 (3,6 %)var multiresistente eller rifampicinresistente tuberkulose (MDR/RR-TB).
TB forårsaket omtrent1,23 millioner dødsfalli 2024, og forble den ledende smittsomme dødsårsaken globalt, og overgikk COVID-19. Etter tre år med økninger mellom 2021 og 2023, falt den globale tuberkuloseforekomsten med nesten 2 % i 2024, noe som gjenspeiler en gradvis gjenoppretting av tuberkulosetjenester.[1]
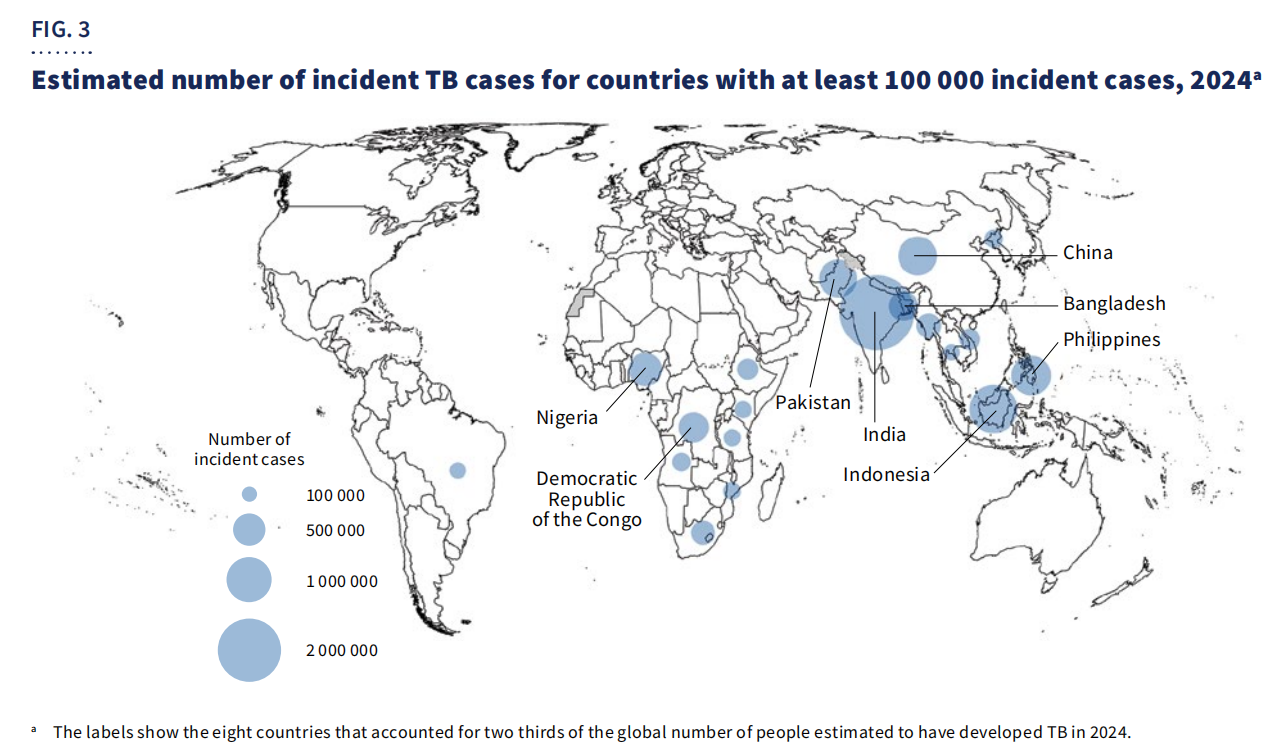
Geografisk sett,67 % av tilfellenevar konsentrert i åtte land: India, Indonesia, Filippinene, Kina, Pakistan, Nigeria, Den demokratiske republikken Kongo og Bangladesh.
Til tross for fremgang er tuberkulose fortsatt en ledende dødsårsak blant mennesker som lever med hiv og en viktig bidragsyter til dødelighet knyttet til antimikrobiell resistens. Global finansiering fortsetter å være mangelfull, med bare5,9 milliarder amerikanske dollartilgjengelig i 2024 – langt underÅrlig mål på 22 milliarder dollarsatt til 2027.
Disse tallene understreker det presserende behovet for å styrke TB-kontrollprogrammer globalt, med fokus på å utvide tilgangen til diagnostikk, forbedre behandlingsresultatene og håndtere de sosiale faktorene som driver TB-smitte. TB krever fortsatt robust internasjonalt samarbeid og politisk forpliktelse for å nå målene i strategien mot TB-bekjempelse.
Mycobacterium tuberculosis: Patogenese og klassifisering
Mycobacterium tuberculosis (MTB/M. tuberculosis) er det primære og vanligste patogenet som forårsaker tuberkulose (TB). Det kan komme inn i menneskekroppen gjennom luftveiene, fordøyelseskanalen eller skadet hud og slimhinner, infisere flere organer og forårsake forskjellige former for TB. Lunge-TB, som hovedsakelig overføres gjennom dråper, står for mer enn 80 % av TB-tilfellene. Vanlige symptomer inkluderer hoste, sputumproduksjon og hemoptyse. Etter infeksjon i lungene kan bakteriene spre seg gjennom blodbanen til flere systemer, noe som potensielt kan føre til skjelett-, urinveis- eller gastrointestinal TB.[2]
MTB er en del av slekten Mycobacterium, som inkluderer:
- Mycobacterium tuberculosis-komplekset (MTBC): Består blant annet av M. tuberculosis, M. bovis, M. africanum, M. canettii og M. microti. Selv om M. tuberculosis er hovedårsaken til tuberkulose, kan M. bovis og M. africanum også indusere sykdommen.
- Ikke-tuberkuløse mykobakterier (NTM).
- Mycobacterium leprae, årsaken til spedalskhet.
Laboratoriediagnostiske tilnærminger
Nøyaktig og rettidig diagnose er avgjørende for effektiv TB-kontroll. Verdens helseorganisasjon understreker atRaske molekylære diagnostiske teknologier har fundamentalt forvandlet tuberkulosedeteksjon ved å muliggjøre svært sensitiv og spesifikk identifisering av patogener samtidig som de oppdager medikamentresistens[1].
- Mikroskopi og kulture: Kultur er fortsatt gullstandarden for TB-diagnose, ettersom den muliggjør definitiv identifisering av levedyktige organismer og støtter testing av medikamentfølsomhet og genomisk analyse. På grunn av den langsomme vekstraten til Mycobacterium tuberculosis, krever imidlertid resultatene vanligvis 2–8 uker, noe som begrenser den kliniske nytten i hastebeslutninger.
-Immunologisk testing: Immunologiske metoder, inkludert tuberkulinhudtesten (TST) og interferon-gamma-frigjøringsanalyser (IGRA), oppdager vertens immunresponser på TB-infeksjon. Selv om disse analysene er nyttige for å identifisere latent infeksjon, kan de ikke pålitelig skille mellom aktiv og tidligere infeksjon, og har derfor begrenset diagnostisk spesifisitet i situasjoner med høy belastning.
-Molekylær diagnostikk (NAAT): DNA-baserte tester som nukleinsyreamplifisering (NAAT) anbefales på grunn av deres høye sensitivitet og spesifisitet.
-Målrettet neste generasjons sekvensering (tNGS): Målrettede sekvenseringsteknologier gir høyoppløselig identifisering av resistensassosierte mutasjoner. WHOs retningslinjer anbefaler tNGS som et avansert verktøy for påvisning av legemiddelresistens etter diagnose, og støtter presise behandlingsstrategier [3].
-Metagenomisk neste generasjons sekvensering (mNGS): Metagenomisk sekvensering muliggjør objektiv deteksjon av et bredt spekter av patogener uten forutgående målvalg. Denne tilnærmingen er spesielt verdifull i komplekse eller uklare kliniske scenarier, inkludert blandede infeksjoner og immunkompromitterte pasienter, der konvensjonell diagnostikk kan være utilstrekkelig.
WHO fremhever videre at mikrobiologisk bekreftelse er avgjørende for å igangsette passende behandling og forbedre pasientutfall, noe som forsterker viktigheten av å integrere avansert molekylærdiagnostikk i TB-kontrollprogrammer [1].
Omfattende molekylære diagnostiske løsninger fra Macro & Micro-Test
1.Multiplex PCR-deteksjon for tuberkulose og medikamentresistenstuberkulose
| Produktkode | Produktnavn | Sertifisering |
| HWTS-RT001 | DNA-deteksjonssett for Mycobacterium Tuberculosis (fluorescens-PCR) | CE |
| HWTS-RT137 | Mycobacterium Tuberculosis Isoniazid-resistensmutasjonsdeteksjonssett (smeltekurve) | CE |
| HWTS-RT074 | Mycobacterium Tuberculosis Nukleinsyre- og Rifampicinresistensdeteksjonssett (smeltekurve) | CE |
| HWTS-RT102 | Nukleinsyredeteksjonssett basert på enzymatisk probe-isotermisk amplifisering (EPIA) for Mycobacterium tuberculosis | CE |
| HWTS-RT144 | Frysetørket Mycobacterium Tuberculosis Complex nukleinsyredeteksjonssett (enzymatisk probe isotermisk amplifisering) | CE |
| HWTS-RT105 | Frysetørket Mycobacterium Tuberculosis DNA-deteksjonssett (fluorescens-PCR) | CE |
| HWTS-RT147 | Mycobacterium Tuberculosis Nukleinsyre og Rifampicin, Isoniazid-resistensdeteksjonssett (smeltekurve) | CE |
Når det er en sterk klinisk mistanke om tuberkulose (TB),HWTS-RT147Testen anbefales for kvalitativ påvisning av MTB-infeksjon og multiresistent tuberkulose (MDR-TB). Denne testen identifiserer mutasjoner irpoB-genet, som fører til rifampicin (RIF)-resistens, og mutasjoner ikatG- og InhA-gener, som er assosiert med isoniazid (INH)-resistens. Den gir en effektiv engangstest for både MTB og MDR-TB, og inkluderer intern kvalitetskontroll for å minimere falskt negative resultater, noe som sikrer raske og nøyaktige resultater.
2.PTNseq målrettet sekvensering for respiratoriske patogener og resistensprofilering
| Produktkode | Produktnavn | Spesifikasjon |
| HWKF-TS0001 | PTNseq-sett for genberikelse av blodomløpsinfeksjonspatogener | 24 tester/sett |
| HWKF-TS0002 | PTNseq Genberikelsessett for infeksjon i sentralnervesystemet, patogene mikroorganismer | 24 tester/sett |
| HWKF-TS0003 | PTNseq-sett for anriking av patogengen for luftveisinfeksjoner | 24 tester/sett |
| HWKF-AT0003 | PTNseq Automatisert berikelsesbiblioteksbyggesett (ONT) for patogene mikroorganismer i luftveisinfeksjoner | 24 tester/sett |
| HWKF-TS0004 | PTNseq bredspektrede genberikelsessett for infeksiøse patogener | 24 tester/sett |
| HWKF-TS0005 | PTNseq Ultra-bredspektret genberikelsessett for infeksiøse patogene mikroorganismer | 24 tester/sett |
| HWKF-TS0151 | Mycobacterium-typing og medikamentresistensgenberikelsessett (multiple amplifiseringsmetode) | 24 tester/sett |
Ved blandede luftveisinfeksjoner (inkludert øvre og nedre luftveisinfeksjoner, tuberkulose og kroniske luftveissykdommer), eller når analyse av legemiddelresistensgen er nødvendig (f.eks. mistanke om legemiddelresistent tuberkulose),PTNseq-serie med målrettet gendeteksjon med høy gjennomstrømningkan anvendes. PTNseq er basert på avansert målrettet sekvenseringsteknologi og benytter ultramultipleks PCR for å berike spesifikke målsekvenser, kombinert med høykapasitetssekvensering og tredjegenerasjons nanoporeteknologi for omfattende patogenidentifikasjon og profilering av legemiddelresistens.
Systemet bruker patenterte, høyspesifisitetsprimere for ultramultipleksamplifisering av målgener. Støttet av en proprietær database og intelligente bioinformatiske algoritmer, gir det nøyaktig patogenidentifikasjon sammen med analyse av medikamentresistens og virulensgen. Målrettet anrikning reduserer interferens fra verts-DNA, forbedrer følsomheten i prøver med høy menneskelig bakgrunn og muliggjør effektiv deteksjon av vanskelige mål somMycobacterium tuberculosis, sopp, intracellulære bakterier, RNA-virus og resistens- eller virulensgener.
PTNseq oppnår en deteksjonsgrenseså lavt som 100 kopier/mlog dekker175 vanlige luftveispatogener, inkludert 76 bakterier, 73 virus, 19 sopp, 7 mykoplasmer, samtKlamydia, Rickettsiaog 54 gener for medikamentresistensPanelet inkludererMycobacterium tuberculosiskomplekse og store ikke-tuberkuløse mykobakterier.
PTNseq-serien kombinerer høy følsomhet med kostnadseffektivitet, forbedrer patogendeteksjonsrater og støtter individualisert antimikrobiell behandling, samtidig som den bidrar til å redusere antimikrobiell resistens. Integrert med det helautomatiske gensekvenseringsbibliotekprepareringssystemet (AIOS) gir den en strømlinjeformet løsning på sykehus med en behandlingstid på så lite som 6,5 timer fra prøve til resultat.

3. Metagenomisk sekvensering for bredspektret patogendeteksjon
| Produktkode | Produktnavn | Spesifikasjon |
| HWKF-MN0011 | Metagenomisk patogendeteksjonssett (DNA-Illumina) | 24 tester/sett |
| HWKF-MN0018 | Metagenomisk patogendeteksjonssett (DNA-MGI) | 24 tester/sett |
| HWKF-MN0021 | Metagenomisk patogendeteksjonssett (DNA-ONT) | 24 tester/sett |
| HWKF-MN0012 | Metagenomisk patogendeteksjonssett (RNA-Illumina) | 24 tester/sett |
| HWKF-MN0019 | Metagenomisk patogendeteksjonssett (RNA-MGI) | 24 tester/sett |
| HWKF-MN0022 | Metagenomisk patogendeteksjonssett (RNA-ONT) | 24 tester/sett |
| HWKF-MN0013 | Metagenomisk patogendeteksjonssett (DNA + RNA-Illumina) | 24 tester/sett |
| HWKF-AYM0013 | Metagenomisk patogendeteksjon Automatisert bibliotekkonstruksjon KiT (DNA+RNA-Illumina) | 24 tester/sett |
| HWKF-MN0020 | Metagenomisk patogendeteksjonssett (DNA+RNA-MGI) | 24 tester/sett |
| HWKF-MN0023 | Metagenomisk patogendeteksjon Kitt (DNA+RNA-ONT) | 24 tester/sett |
Når den kliniske diagnosen er uklar,mNGS-patogen med høy gjennomstrømningsgendeteksjonkan utføres på ulike prøver fra pasienten, inkludert bronkoalveolær skyllevæske, sputum, halsprøver, blod, pleuraeffusjon, puss og vevsprøver. Denne tilnærmingen bruker metagenomisk sekvenseringsteknologi, der ulike prøver gjennomgår målrettet forbehandling etterfulgt av nukleinsyreekstraksjon ved bruk av glasskuler og veggfordøyende enzymer, noe som forbedrer ekstraksjonseffektiviteten. Sekvenseringen er tilpasset flere plattformer, noe som sikrer et høyt datavolum for forbedret mNGS-følsomhet og monteringsintegritet. Dataene analyseres ved hjelp av en egenbygd database og intelligente algoritmer for å oppdageover 20 000 patogener, inkludert bakterier, sopp, virus og parasitter, og gir informasjon om mistenkte patogene mikroorganismer. Denne metoden er egnet for vanskelig diagnostiserende, kritisk syke eller immunkompromitterte pasienter, inkludert identifisering avTerrengsykkelkompleksogNTM, så vel som blandede infeksjoner. Det forbedrer patogendeteksjonsratene betydelig og bidrar til å veilede klinisk målrettet antibiotikabruk, noe som muliggjør presis infeksjonsdiagnose.
Konklusjon
Selv om det er gjort betydelige fremskritt, er tuberkulose fortsatt en stor global helseutfordring, spesielt i sammenheng med medikamentresistens, finansieringshull og ulik tilgang til diagnostikk.
WHO understreker at det å oppskalere tilgangen til rask molekylærdiagnostikk og avanserte sekvenseringsteknologier er avgjørende for å nå målene i strategien for å avskaffe tuberkulose. Med fortsatt innovasjon, investeringer og globalt samarbeid er det å avskaffe tuberkulose ikke lenger en ambisjon, men et oppnåelig mål.
Referanser:
- Verdens helseorganisasjon. Global tuberkuloserapport 2024/2025: Diagnostisk testing og behandling.
- Verdens helseorganisasjon. WHOs håndbok for valg av molekylære WHO-anbefalte hurtigdiagnostiske tester for påvisning av tuberkulose og medikamentresistent tuberkulose.
- Verdens helseorganisasjon. WHOs konsoliderte retningslinjer for tuberkulose: Modul 3 – Diagnose (oppdatering 2024).
Publisert: 24. mars 2026
