1 Bakgrunn for dengueepidemien: En eskalerende global folkehelseutfordring
Dengue er en akutt myggbåren virussykdom forårsaket av dengueviruset (DENV), som har blitt den raskest spredende arbovirussykdommen globalt, og utgjør en betydelig trussel mot folkehelsesikkerheten. I løpet av de siste to tiårene har den globale forekomsten av dengue økt dramatisk, med antallet rapporterte tilfeller som har doblet seg årlig siden 2021 [1]. I desember 2023 erklærte Verdens helseorganisasjon (WHO) en global dengue-krise for å styrke koordinert internasjonal responsinnsats. Epidemiologiske estimater fra WHO indikerer at omtrent 3,9 milliarder individer over hele verden er i faresonen for dengueinfeksjon, med anslagsvis 390 millioner infeksjoner som forekommer årlig – hvorav 96 millioner presenterer seg som klinisk synlige tilfeller [1,2].
2 epidemiologiske høydepunkter
De epidemiologiske egenskapene til denguefeber formes av samspillet mellom virologiske faktorer, vektorøkologi, vertens immunresponser og sosio-miljømessige forhold. En omfattende forståelse av disse egenskapene er avgjørende for utvikling av effektive forebyggings- og kontrollstrategier samt nøyaktige diagnostiske tilnærminger.
2.1 Overføringsvektorer og urbane overføringsmønstre
Dengueviruset overføres hovedsakelig viaAedes aegypti og Aedes albopictusmygg. Blant disse vektorartene er Aedes aegypti anerkjent som den mest kritiske overføringsvektoren, karakterisert ved høy "menneskelig tilpasningsevne" og utbredt distribusjon i tropiske og subtropiske bymiljøer. I motsetning til andre myggvektorer av arbovirale patogener, viser Aedes aegypti følgende viktige epidemiologiske egenskaper:
-En preferanse for avl i menneskeskapte miljøer (f.eks. vannlagringsbeholdere, kasserte dekk)
-En sterk tropisme for menneskeblod som næringskilde
-Fôringsatferd på dagtid
Disse trekkene definerer dengue som en typisk«smittsom sykdom i byen»med betydelig økt overføringseffektivitet i tettbygde områder. WHO-relaterte studier har vist at i urbane områder med høy befolkningstetthet kan økt hyppighet av mygg-menneskelig kontakt øke det grunnleggende reproduksjonstallet (R₀) for DENV betydelig, og dermed akselerere spredningen av epidemier [2].
2.2 Globale spredningstrender og drivende faktorer
Ifølge WHO-rapporter har det globale antallet rapporterte denguetilfeller økt eksponentielt de siste to tiårene [1,3]. Denne oppadgående trenden er primært drevet av følgende sammenkoblede faktorer:
(1) Klimaendringer: Stigende globale temperaturer utvider ikke bare det geografiske området for egnede habitater for myggvektorer, men forkorter også den ytre inkubasjonsperioden for DENV i myggverten, og forbedrer dermed overføringseffektiviteten. Klimainduserte variasjoner i myggtetthet har blitt validert av WHO som en pålitelig prediktor for den spatiotemporale dynamikken i dengueutbrudd.
(2) Urbanisering: Rask og uplanlagt byutvidelse har skapt rikelig med ynglehabitater for myggvektorer, mens økt befolkningstetthet har styrket kontinuiteten i DENV-smittekjedene.
(3) Global befolkningsbevegelse: Internasjonal reisevirksomhet og handel har lagt til rette for rask grenseoverskridende overføring av DENV, og fremmet overgangen fra importerte tilfeller til vedvarende lokal overføring. WHOs overvåkingsdata viser at USA mellom 2010 og 2021 rapporterte 7528 reiserelaterte denguetilfeller, hvorav 3135 krevde sykehusinnleggelse og 19 resulterte i dødelighet.
(4) Utvidelse av vektordistribusjon: Globalt fortsetter det geografiske utbredelsen av Aedes aegypti og Aedes albopictus å utvide seg, og Aedes-mygg etablerer seg stadig mer i deler av Europa. Følgelig har dengue utviklet seg fra en tradisjonelt regional epidemi til en global folkehelsetrussel.
2.3 Mekanismer for ko-sirkulasjon av flere serotyper og reinfeksjon
Denguevirus består av fire antigenisk forskjellige serotyper (DENV-1 til DENV-4). Infeksjon med én serotype gir langvarig beskyttende immunitet mot den spesifikke serotypen, men bare midlertidig og delvis kryssbeskyttelse mot de tre andre serotypene. Den generelle befolkningen er universelt mottakelig for DENV, og bare en undergruppe av infiserte individer utvikler klinisk sykdom [2].
I endemiske regioner sirkulerer ofte flere DENV-serotyper samtidig, noe som resulterer i potensialet for at individer kan oppleve flere dengueinfeksjoner i løpet av livet. WHOs epidemiologiske studier har identifisert multiserotype-ko-sirkulasjon som en viktig årsak til periodiske dengueutbrudd [1].
2.4 Sekundærinfeksjon og antistoffavhengig forsterkning
Et kritisk og unikt fenomen innen dengueepidemiologi erantistoffavhengig forsterkning (ADE)Under sekundærinfeksjon med en heterolog DENV-serotype, letter ikke-nøytraliserende antistoffer produsert under den primære infeksjonen virusets inntreden i monocytter og makrofager, og forbedrer dermed virusreplikasjonen. Denne mekanismen er bredt anerkjent av WHO som en viktig patogen faktor ved alvorlig denguefeber, inkludert hemoragisk denguefeber og denguesjokksyndrom [1].
WHOs epidemiologiske data viser konsekvent at personer med sekundær dengueinfeksjon har en betydelig høyere risiko for å utvikle alvorlig sykdom sammenlignet med de med primærinfeksjon – en egenskap som er av stor betydning for sykdomsovervåking og klinisk behandling. Det er viktig å merke seg at selv om risikoen for alvorlig sykdom er forhøyet under sekundærinfeksjon, kan infeksjon med enhver DENV-serotype potensielt utvikle seg til alvorlig dengue [1].
2.5 Uspesifikke kliniske manifestasjoner og risiko for feildiagnose
De kliniske manifestasjonene av denguefeber er bemerkelsesverdig uspesifikke, spesielt i de tidlige stadiene av sykdommen, og overlapper ofte med andre myggbårne virusinfeksjoner (f.eks. chikungunya- og Zika-virus) samt visse luftveisinfeksjoner. WHO-estimater indikerer at 40–80 % av DENV-infeksjoner er asymptomatiske [3].
Typiske kliniske manifestasjoner inkluderer:
-Akutt feber (vedvarer i 2–7 dager, kan være tofaset)
-Alvorlig hodepine og retroorbital smerte (smerter bak øynene)
-Muskel- og leddsmerter (ofte omtalt som «beinsbruddsfeber»)
-Makulært eller makulopapulært utslett
-Mild hemoragisk manifestasjon (f.eks. ekkymose, epistaksis, tannkjøttblødning)
Symptomatisk denguefeber deles vanligvis inn i tre distinkte faser: feberfasen, den kritiske fasen og rekonvalesensfasen. Omtrent mindre enn 5 % av symptomatiske pasienter utvikler alvorlig denguefeber. På grunn av mangelen på spesifikke kliniske trekk er diagnose basert utelukkende på kliniske symptomer utfordrende, noe som øker risikoen for feildiagnose og underdiagnose. WHO understreker eksplisitt at klinisk diagnose alene ikke er tilstrekkelig for å sikre nøyaktighet, noe som gjør laboratoriebekreftelse uunnværlig [1].
3 viktige punkter fra WHO «Laboratorietesting for denguevirus: Midlertidig veiledning, april 2025»
I april 2025 publiserte Verdens helseorganisasjon oppdaterte, midlertidige retningslinjer for laboratorietesting for DENV, som gir autoritativ teknisk veiledning for global denguediagnose. Denne veiledningen syntetiserer den nyeste bevisen på laboratorietesting av dengue i sammenheng med den pågående globale denguekrisen og tilbyr praktiske anbefalinger skreddersydd for miljøer med varierende ressursnivåer.

3.1 Grunnleggende prinsipper for teststrategi
Veiledningen understreker at denguediagnose må benytte en kombinert teststrategi med flere markører basert på sykdomsstadiet [1]. Gitt fraværet av en universell diagnostisk algoritme, bør teststrategiene tilpasses lokale epidemiologiske kontekster, med hensyn til følgende nøkkelfaktorer [1]:
-Infeksjonsstadium: Antall dager etter symptomdebut avgjør den mest passende testmetoden.
-Prøvetype: Egnetheten til fullblod, plasma eller serum for DENV-deteksjon
-Regional epidemiologi: De lokalt sirkulerende DENV-serotypene og ko-sirkulasjon av andre arbovirus
-Risiko for koinfeksjon: I regioner med overlappende arbovirus-sirkulasjon bør multiplekstesting vurderes for å skille mellom ulike patogener.
3.2 Fasebasert teststrategi
I følge WHOs retningslinjer bør laboratorietesting av dengue følge klare tidsvinduer basert på sykdomsstadiet [1,2]:
(1) Akuttfasetesting (≤7 dager etter debut)
-Nukleinsyretesting (molekylær testing): Omvendt transkripsjon-polymerasekjedereaksjon (RT-PCR) og andre molekylære metoder påviser DENV RNA med høy følsomhet.
-Antigentesting: NS1-antigendeteksjon, som blir påvisbar innen 1–3 dager etter debut.
I den akutte fasen er vireminivåene relativt høye, og testing av nukleinsyre og antigen oppnår optimal sensitivitet.
(2) Testing i rekonvalesensfasen (≥4 dager etter debut)
-Serologisk testing: IgM-antistoffer blir vanligvis påviselige rundt dag 4 etter debut.
-I de fleste tilfeller vedvarer IgM-antistoffer i 14–20 dager, og i noen tilfeller kan vedvarelsen vare i opptil 90 dager.
-IgG-testing har begrenset verdi for diagnose av akutt denguefeber på grunn av potensielle kryssreaktive antistoffer fra tidligere flavivirusinfeksjon eller vaksinasjon.
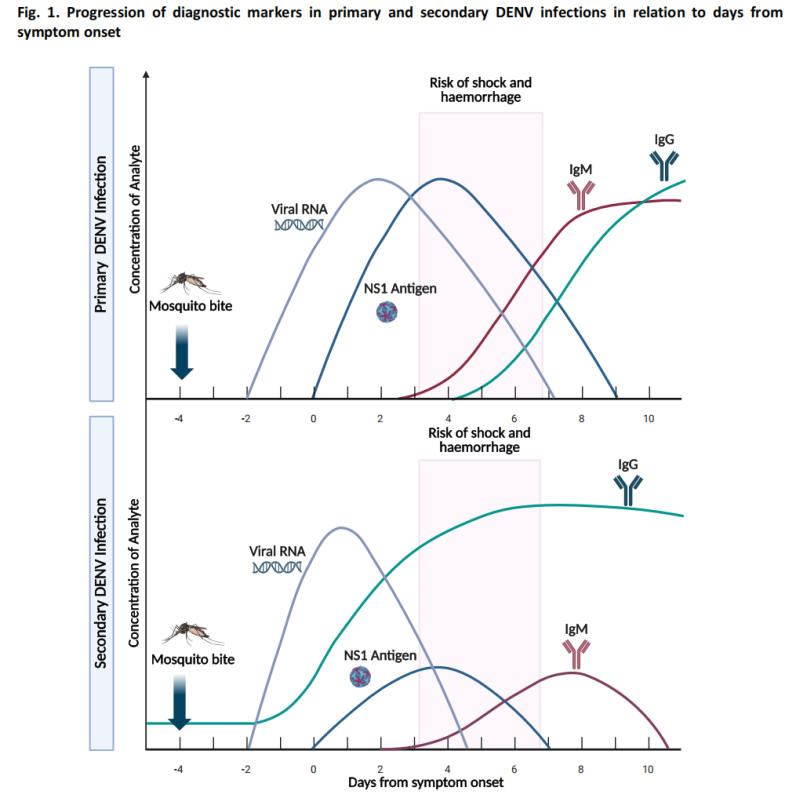
(3) Algoritme for diagnostikk av mistenkte tilfeller
Veiledningen inkluderer en diagnostisk algoritme for mistenkte denguetilfeller, og anbefaler passende testmetoder basert på dager etter symptomdebut: NS1-antigentesting og nukleinsyretesting er de primære tilnærmingene i den tidlige fasen, mens serologisk testing er den primære metoden i den senere fasen.
3.3 Evaluering og valg av testmetodeytelse
Ifølge WHO er en systematisk evaluering av ytelsen og gjeldende scenarier for ulike denguetestinger som følger:
| Testmetode | Mål | Tidsvindu | Primært applikasjonsscenario | Hensyn |
| Nukleinsyretesting | Viralt RNA | 1–7 dager etter debut | Tidlig bekreftelse, serotypeidentifikasjon | Gullstandardmetode; krever spesialisert laboratorieutstyr og teknisk ekspertise |
| NS1-antigentesting | Ikke-strukturelt protein | 1–3 dager etter debut | Tidlig hurtigscreening | Tilgjengelig i hurtigdiagnostisk testformat (RDT), egnet for ressursbegrensede miljøer |
| IgM-antistofftesting | Spesifikke IgM-antistoffer | ≥4 dager etter debut | Diagnose av nylig infeksjon | En enkelt serumprøve antyder bare en mulig nylig infeksjon; serokonversjon er nødvendig for bekreftelse |
| IgG-antistofftesting | Spesifikke IgG-antistoffer | Rekonvalesent/tidligere infeksjon | Epidemiologisk undersøkelse, vurdering av immunitetsstatus | En enkelt serumprøve er ikke egnet for diagnose av akutt denguefeber |
| Kombinert testing (NS1+IgM/IgG) | Antigen + antistoffer | Fullstendig sykdomsforløp | Omfattende diagnose av dengueinfeksjon | For tiden det best ytende RDT-formatet for denguediagnose |
| NGS | Viralt RNA | 1–7 dager etter debut | Viral genomisk overvåking | Krever spesialisert sekvenseringsutstyr og bioinformatiske analysemuligheter |
4 anbefalinger for makro- og mikrotesting av denguedeteksjonsprodukter etter scenario
For å støtte forebygging og kontroll av denguefeber tilbyr Macro & Micro-Test en integrert diagnostisk portefølje som dekker rask screening, molekylær bekreftelse og genomisk overvåking, og dekker behov på tvers av ulike stadier av utbruddshåndtering.
4.1 Scenario 1: Rask screening og målrettet overvåking
Gjelder feberklinikker, primærhelsetjenester, screening i lokalsamfunnet for utbrudd og karantene i havner/på grensen.
-Denguevirus NS1-antigenhurtigtest: Oppdager tidlig infeksjon (1–3 dager etter debut) med resultater etter 15 minutter for rask sortering.
-Denguevirus IgM/IgG-antistofftest: Skiller mellom primære/sekundære infeksjoner for å evaluere alvorlig sykdomsrisiko.
-Denguevirus NS1-antigen + IgM/IgG kombinert hurtigtest: Detekterer antigen og antistoffer samtidig for fullstendig diagnose.
-Chikungunya-virus IgM/IgG-antistofftest: Muliggjør differensialdiagnose med denguefeber for å identifisere patogener nøyaktig.
4.2 Scenario 2: Presisjonsdiagnose og nødrespons
-Denguevirus I/II/III/IV nukleinsyredeteksjonssett: Oppdager og differensierer 4 serotyper (deteksjonsgrense 500 kopier/ml) for sporing av utbrudd.
-Lyofilisert PCR-sett for denguevirus: Kan transporteres i romtemperatur, egnet for ressursbegrensede områder og plutselige utbrudd.
-Dengue/Zika/Chikungunya Multiplex Real-Time PCR Kit: Oppdager samtidig 3 arbovirus for effektiv differensialdiagnose ved komplekse utbrudd.

Alle reagensene ovenfor er kompatible med AIO 800 helautomatiserte prøve-til-svar-system, noe som reduserer manuell betjening og krysskontaminering, og forbedrer effektivitet og biosikkerhet.
4.3 Scenario 3: Genomisk overvåking og analyse av virusavstamning
Gjelder for nasjonale referanselaboratorier og forskningsinstitusjoner innen folkehelse, i samsvar med WHOs posisjonering av NGS.
Macro & Micro-Tests genomiske overvåkingsløsninger støtter helgenomsekvensering for virussporing, avklaring av overføringskjeden, variantovervåking og justering av vaksinestrategi. De støtter manuelle/automatiserte arbeidsflyter, forbedrer gjennomstrømning og reproduserbarhet, og gjør det mulig for laboratorier å oppgradere fra rutinetesting til avansert overvåking, i samsvar med WHOs vekt på å styrke overvåkingen av virusutviklingen.

4.4 Verdien av integrerte løsninger
Macro & Micro-Test tilbyr komplette diagnostiske løsninger for påvisning av arbovirus, som støtter hvert trinn i utbruddshåndteringen: raske screeningsverktøy for helsetjenester i frontlinjen, molekylær bekreftelse for presisjonsdiagnose og fullgenomanalysemuligheter for epidemiologisk overvåking. Med høytytende analyser, fleksible arbeidsflyter og automatiseringsklare plattformer, gir disse løsningene laboratorier og folkehelsesystemer mulighet til å styrke beredskapen og responsen på nye arbovirustrusler over hele verden.
Referanser
[1] Verdens helseorganisasjon. Laboratorietesting for denguevirus: Midlertidig veiledning, april 2025. Genève: Verdens helseorganisasjon; 2025.
[2] WHOs globale arbovirusinitiativs tekniske rådgivningsgruppe. Styrking av global beredskap og respons på trusler fra arbovirussykdommer: En oppfordring til handling. Lancet Infect Dis. 2026;26(1):15–17.
[3] Lancet-mikroben. Å overvinne dilemmaet med denguediagnostikk. Lancet-mikroben. 2025;6(7):101190.
Publisert: 20. mars 2026
